92724

Chemia fizyczna - termodynamika molekularna 2009/2010 48
ln(? = ln#-
kT
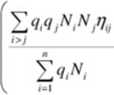
^ i
Wyrażenie na potencjał chemiczny składa się z dwóch udziałów - udziału kombinatorycznego i udziału pochodzącego od energii sieci
pt/kr = -

Dla układu dwuskładnikowego potencjał chemiczny składnika (1) będzie równy
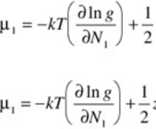
zqxZ\\ + zqlq2NlN2X\t2 zqfiu + zqfllTl,2
+ N2q2 - Nxqx (Nxqx+N2q2)2
Pierwszy wyraz równoważny jest funkcji otrzymanej dla roztworu doskonałego. Stosując zwykły zapis, otrzymamy
p, =pj + /?r In xx + zqfi]r\l2 =p? + y?7'lnjc2 + Ztf20?iJl2
Stąd wyrażenia na współczynniki aktywności RT lny, = zqfi\i\n RT lny, = zqfi]r\l2 A podstawowa funkcja nadmiarowa - G, będzie miała formę GF = RT(.r, lny, + .v2 lny2) = złi12^e,02 gdzie qm=xlql + x2q2
Różnice pomiędzy qi i q2 powodują asymetrię krzywej nadmiarowej entalpii swobodnej w funkcji składu.
Pozostałe funkcje otrzymujemy z różniczkowania:
HF = GF: S* = 0; V* = 0
3. Interpretacja odchyleń od doskonałości.
Znak odchyleń od doskonałości dla roztworu regularnego zależy od znaku energii wymiany. Gh > 0 dla rji2 > 0 (dodatnie odchylenia od doskonałości)
€/2 - 1/2(£// + £22) > 0
Jako energie oddziaływali przyciągających, wartości ą- są mniejsze od zera. Analogiczna nierówność wyrażona przez wartości bezwzględne będzie miała formę
Wyszukiwarka
Podobne podstrony:
Chemia fizyczna - termodynamika molekularna 2009/2010 37 Wykład 10 11.12.2009 1. Równania stanu w te
Chemia fizyczna - termodynamika molekularna 2009/2010 52 Wykład 13 15.01.2010 1. O
Chemia fizyczna - termodynamika molekularna 2009/2010 32 Wykład 9 4.12.2009 1. Uogólniona funkcja po
Chemia fizyczna - termodynamika molekularna 2009/2010 7 6. Przykład z życia. Chcemy znaleźć temperat
Chemia fizyczna - termodynamika molekularna 2009/2010 38 Chemia fizyczna - termodynamika molekularna
Chemia fizyczna - termodynamika molekularna 2009/2010 43 M(xlel roztworu doskonałego jest stosowany
Chemia fizyczna - termodynamika molekularna 2009/2010 53 poprawki i często bywają w ogóle pomijane.
Chemia fizyczna - termodynamika molekularna 2009/2010 8 wnętrze Słońca - 2 000 000 K Czy istnieje sz
Chemia fizyczna • termodynamika molekularna 2009/2010 12 4. W stanic rozważanej równowagi, wszystkie
Chemia fizyczna - termodynamika molekularna 2009/2010 16 występujący w róźnic/cc zupełnej energii
Chemia fizyczna - termodynamika molekularna 2009/2010 20 4. Sprawdzamy ekstensywno
Chemia fizyczna - termodynamika molekularna 2009/2010 25 ć)H dH —— = q.
Chemia fizyczna - termodynamika molekularna 2009/2010 29 Chemia fizyczna - termodynamika molekularna
Chemia fizyczna • termodynamika molekularna 2009/2010 33 Konfiguracyjna funkcja podziału będzie równ
Chemia fizyczna - termodynamika molekularna 2009/2010 1 Wykład 1. 2.10.2009 1. Pla
Chemia fizyczna - termodynamika molekularna 2009/2010 42 Wykładll 18.12.2008 1. Roztwór doskonały w
Chemia fizyczna - termodynamika molekularna 2009/2010 11 Wykład 4 23.10.2009 1.
Chemia fizyczna - termodynamika molekularna 2009/2010 15 Wykład 5 30.10.2009 1. Wa
Chemia fizyczna - termodynamika molekularna 2009/2010 19 Wykład 6 5.11.2009 1. Wątpliwość (wyrażona
więcej podobnych podstron